
Polyneuropathie (pDPN)
Die schmerzhafte diabetische Polyneuropathie(pDPN) ist eine...

Postoperative und posttraumatische neuropathische Schmerzen (PSNP/PNI) entstehen durch Nervenverletzungen bei chirurgischen Eingriffen oder durch Traumata. Sie können einen erheblichen Einfluss auf die Lebensqualität der Betroffenen haben. Zu den Symptomen gehören neben Schmerzen auch Einschränkungen der Lebensqualität sowie auch der mentalen Gesundheit.1
In die Analyse der CASPAR-PSNP-Studie wurden 499 Patienten einbezogen, die unter PSNP und PNI litten, eine bis vier Behandlungen mit QUTENZA® erhalten haben und über einen Zeitraum von 12 Monaten nachverfolgt wurden. Untersucht wurden die Veränderungen der Schmerzintensität im Verlauf der Anwendungen, die Entwicklung der mentalen Gesundheit sowie die Notwendigkeit begleitender Schmerzmedikamente im Laufe wiederholter QUTENZA®-Behandlungen.
Die Studie liefert überzeugende Belege dafür, dass wiederholte Behandlungen mit dem hochdosierten Capsaicin-Pflaster zu einer fortschreitenden Verbesserung der Schmerzintensität bei PSNP führen können. Im Zuge dessen wird auch die Schlafqualität sowie die mentale Gesundheit der Patienten verbessert.
Darüber hinaus unterstreicht die rückläufige Notwendigkeit einer begleitenden Schmerzmedikation das Potenzial von QUTENZA® als hilfreiche Komponente im langfristigen Schmerzmanagement.1
Die durchschnittliche 24-Stunden-Schmerzintensität sank signifikant um 31,0 mm VAS (visuellen Analogskala) nach vier Behandlungen. Bei Patienten, die die Therapie nach einer, zwei oder drei Behandlungen abbrachen kam es zu einer erneuten Zunahme der Schmerzintensität, während bei den Patienten, die die Behandlung fortsetzten, eine weitere Schmerzreduktion eintrat.1
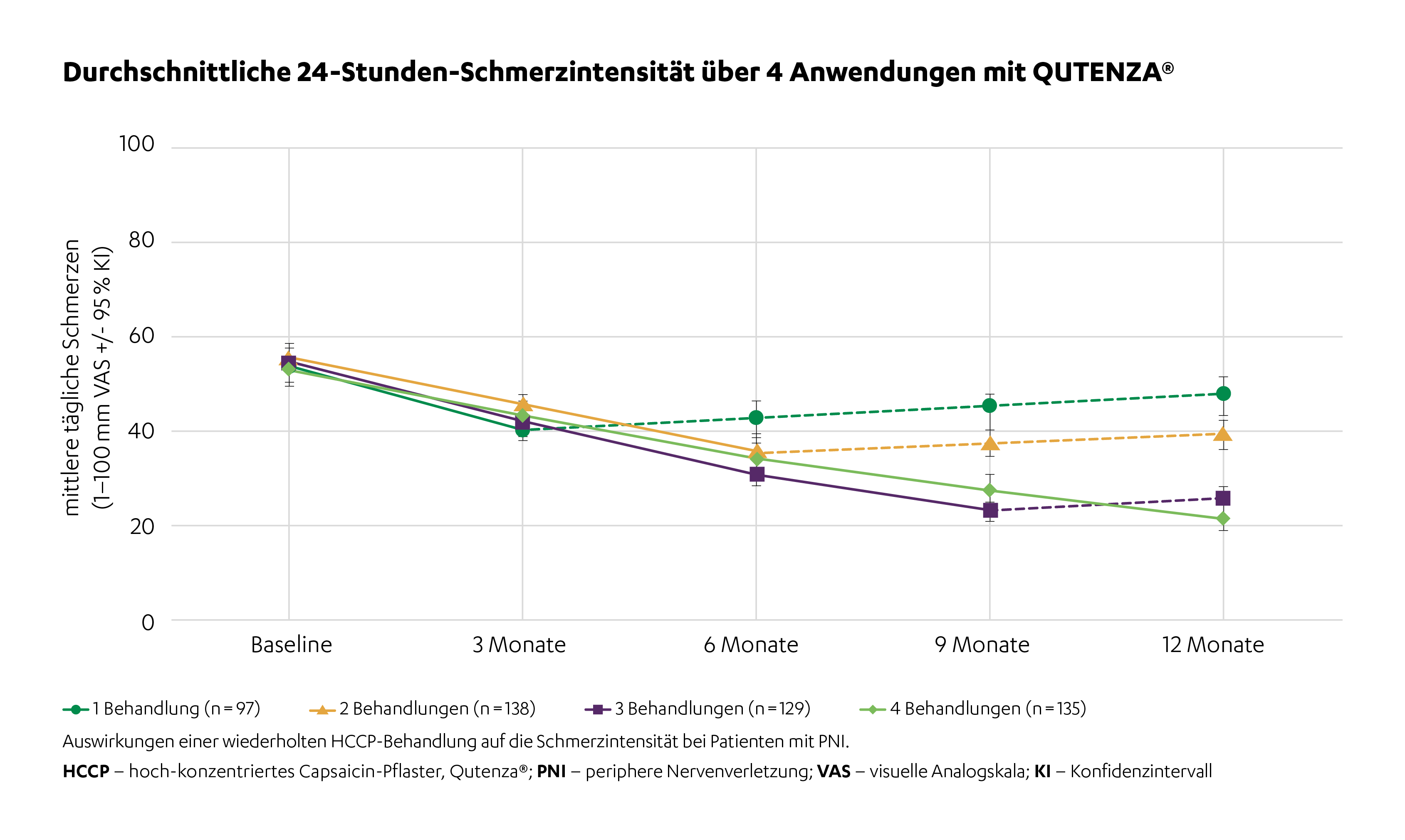
Die Ansprechrate gemessen an einer Schmerzreduktion ≥ 30 % bzw. ≥ 50 % (mm auf der VAS) nahm bei aufeinanderfolgenden Behandlungen kontinuierlich zu. Fast alle Teilnehmenden erreichten dabei eine Schmerzreduktion von ≥ 30 % nach 4 Anwendungen.1
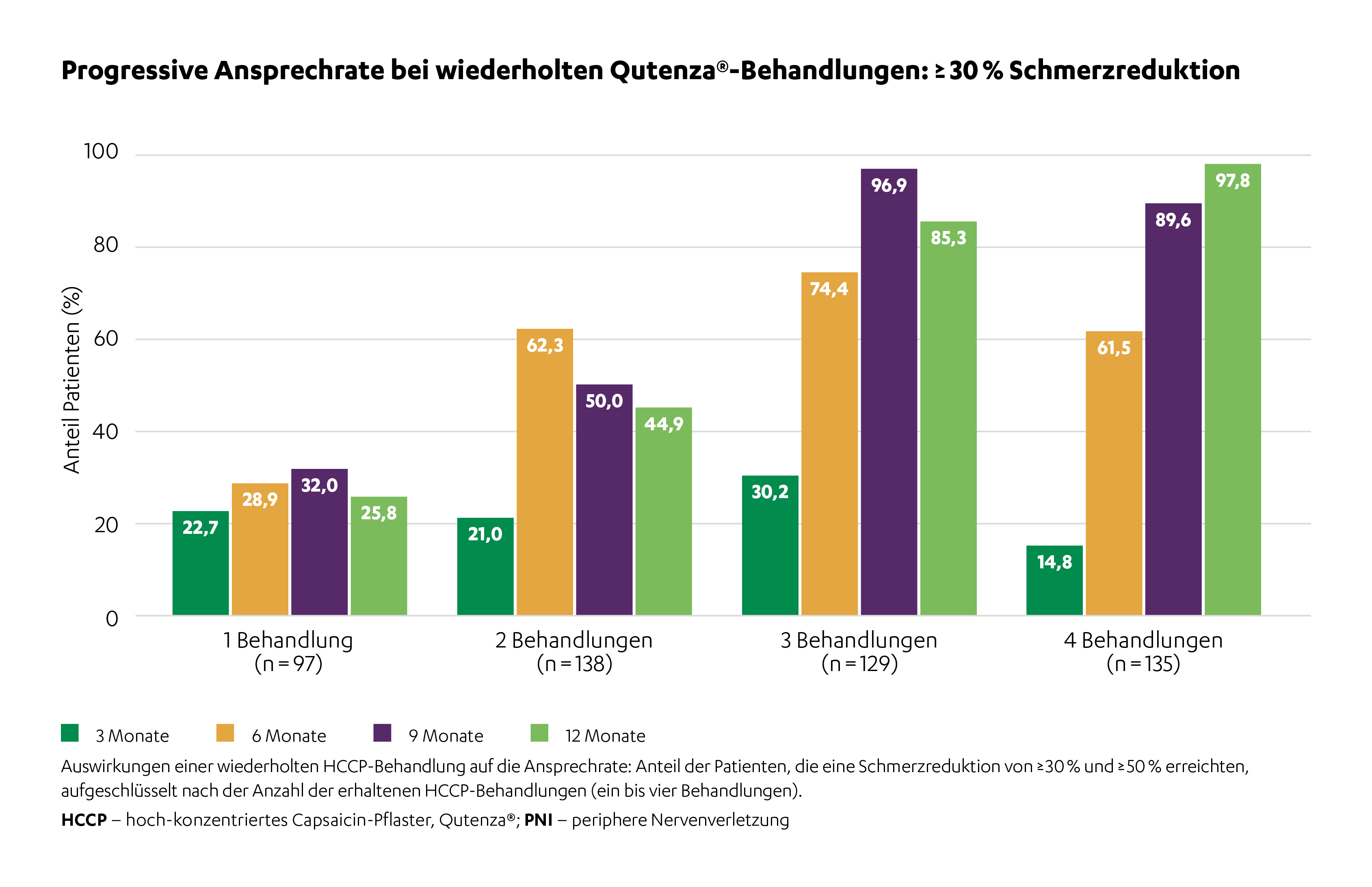
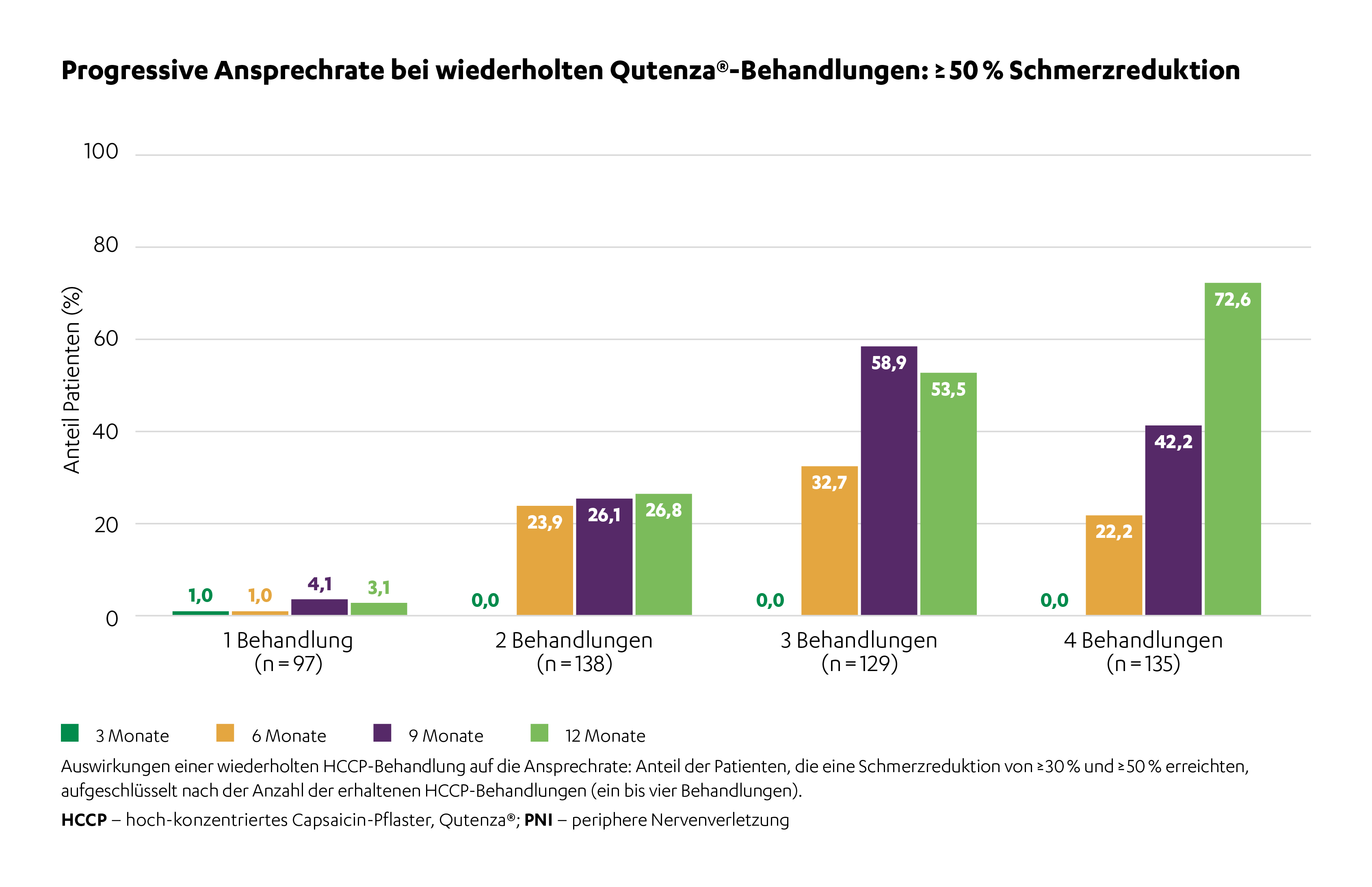
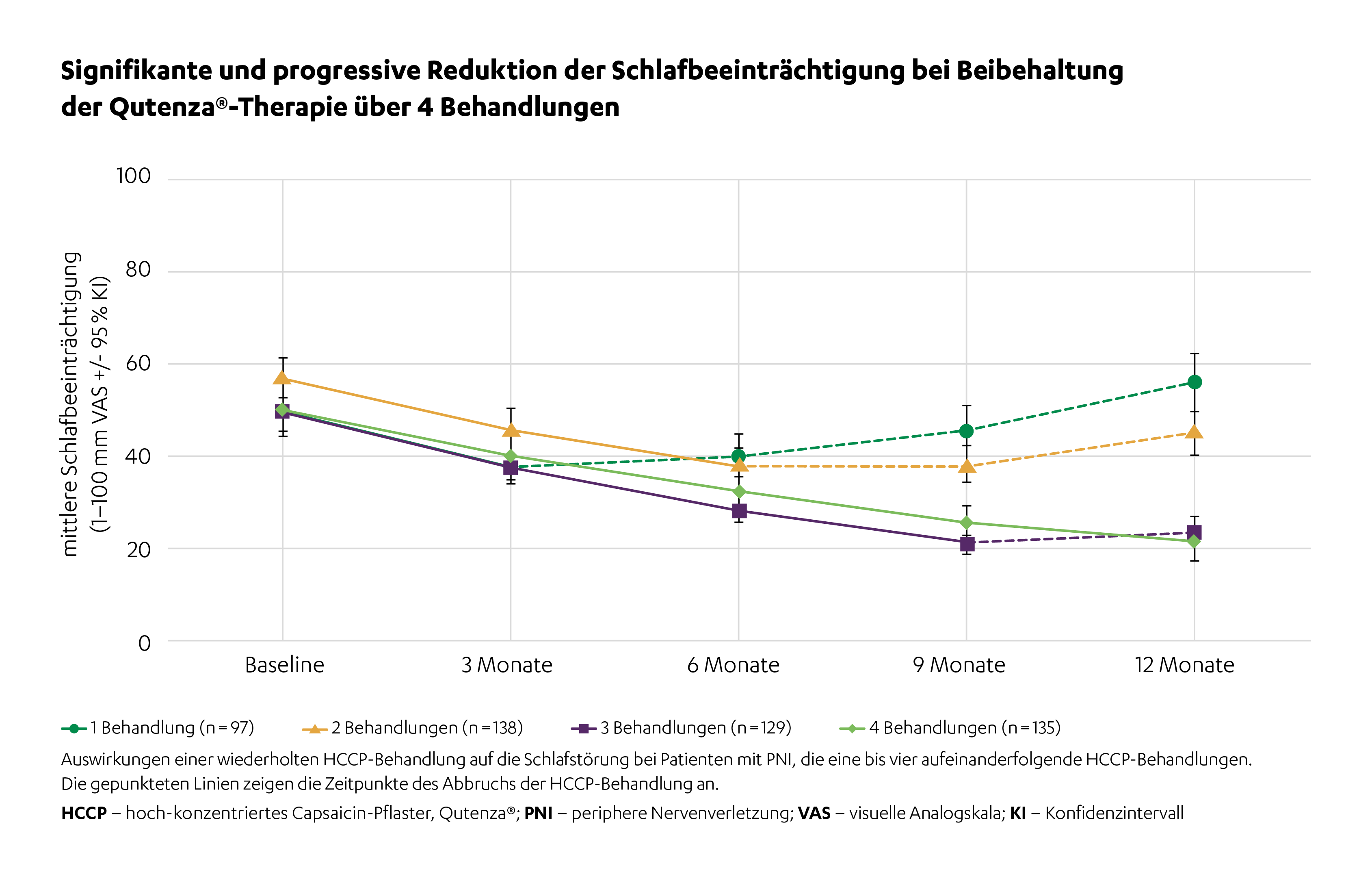
In der Real-World-Evidence Studie nahmen die Schlafstörungen, gemessen am mPDI Schlaf-Score kontinuierlich über vier Behandlungen ab.1
Ergänzend zu den Untersuchungen der Schmerzintensität und Lebensqualität, wurde zusätzlich die Auswirkung der Mehrfachanwendung von QUTENZA® auf die begleitende Schmerzmedikation von den Patienten analysiert.1
Alle Patienten nahmen zu Beginn der Studie orale Schmerzmedikamete ein wie Antidepressiva, Antikonvulsiva und starke Opioide. Über den Verlauf von vier Anwendungen nahm der Anteil Patienten, die diese Medikamente einnahmen um 46%, 28% beziehungsweise 36% ab.1
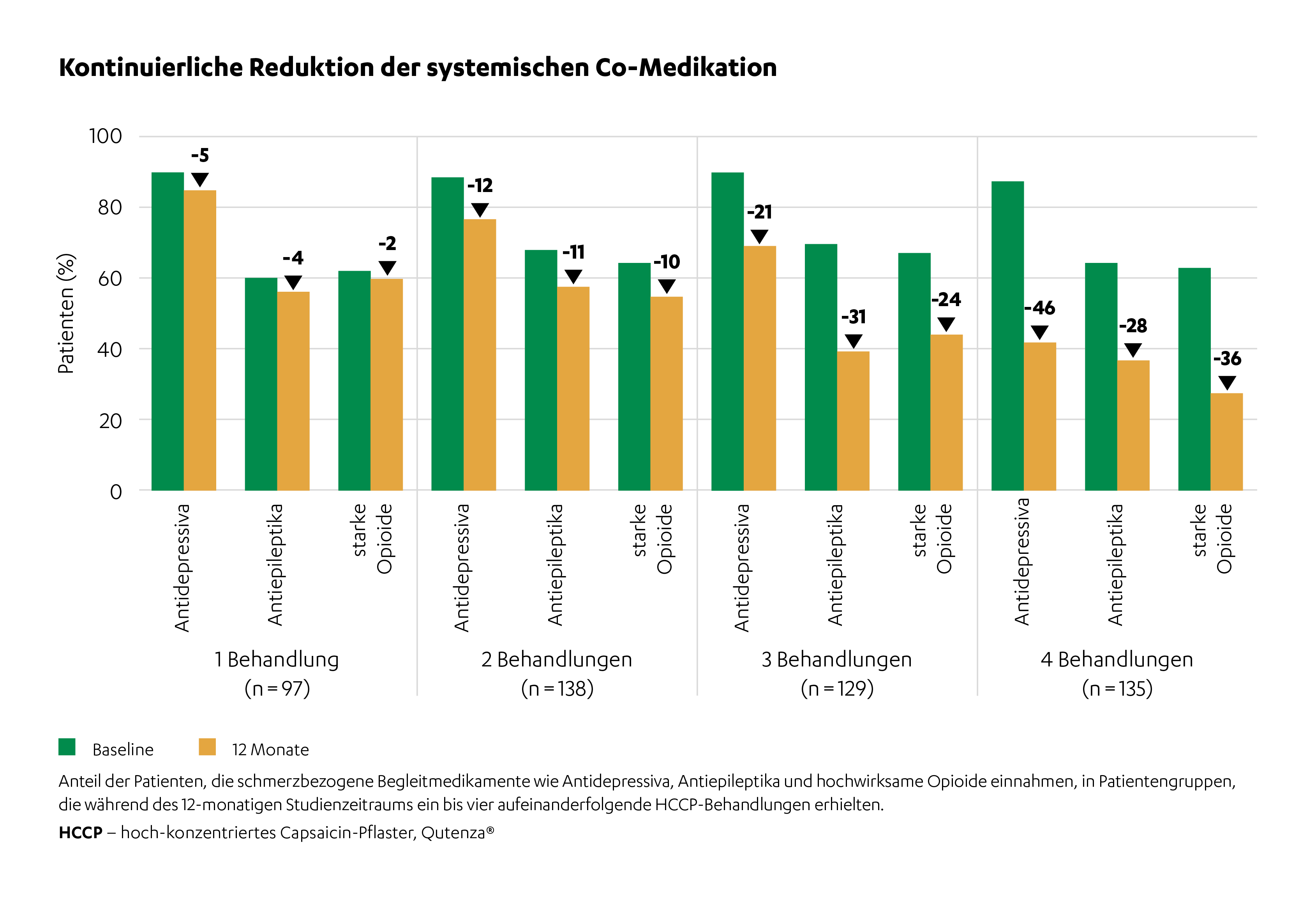
Insgesamt nahm die Co-Medikation von vier durchschnittlich eingenommenen Medikamenten um 2,2 ab nach vier Behandlungen.1
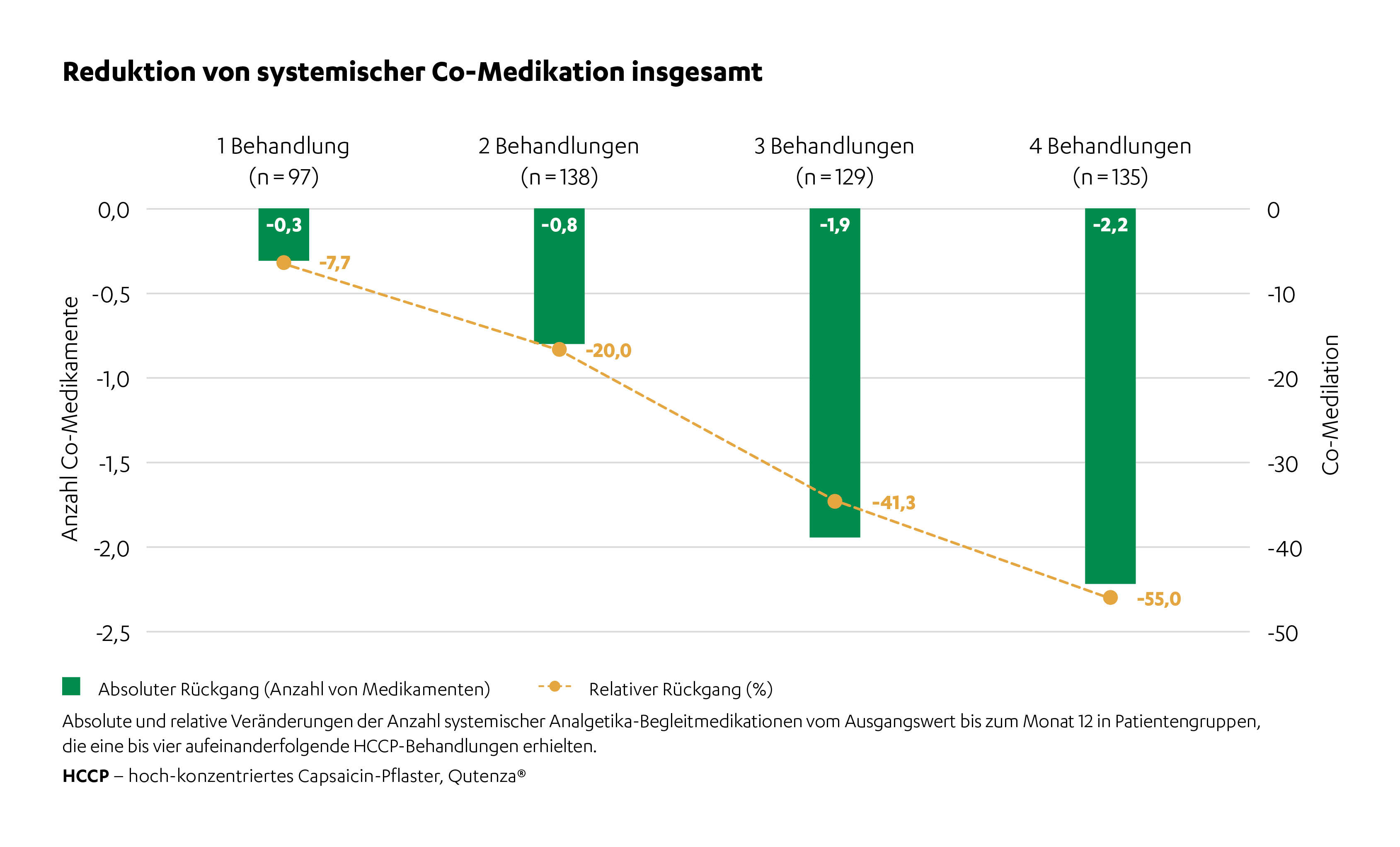
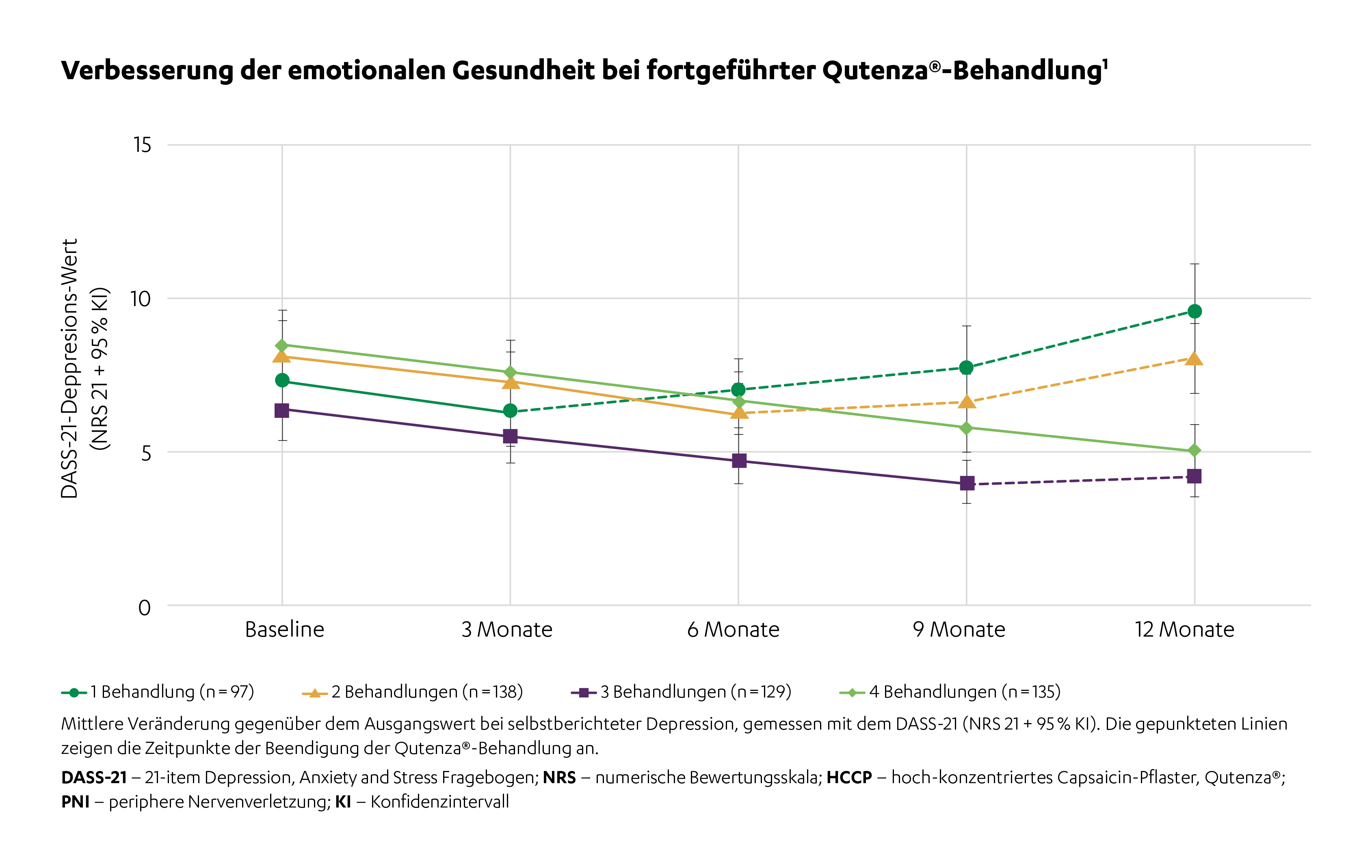
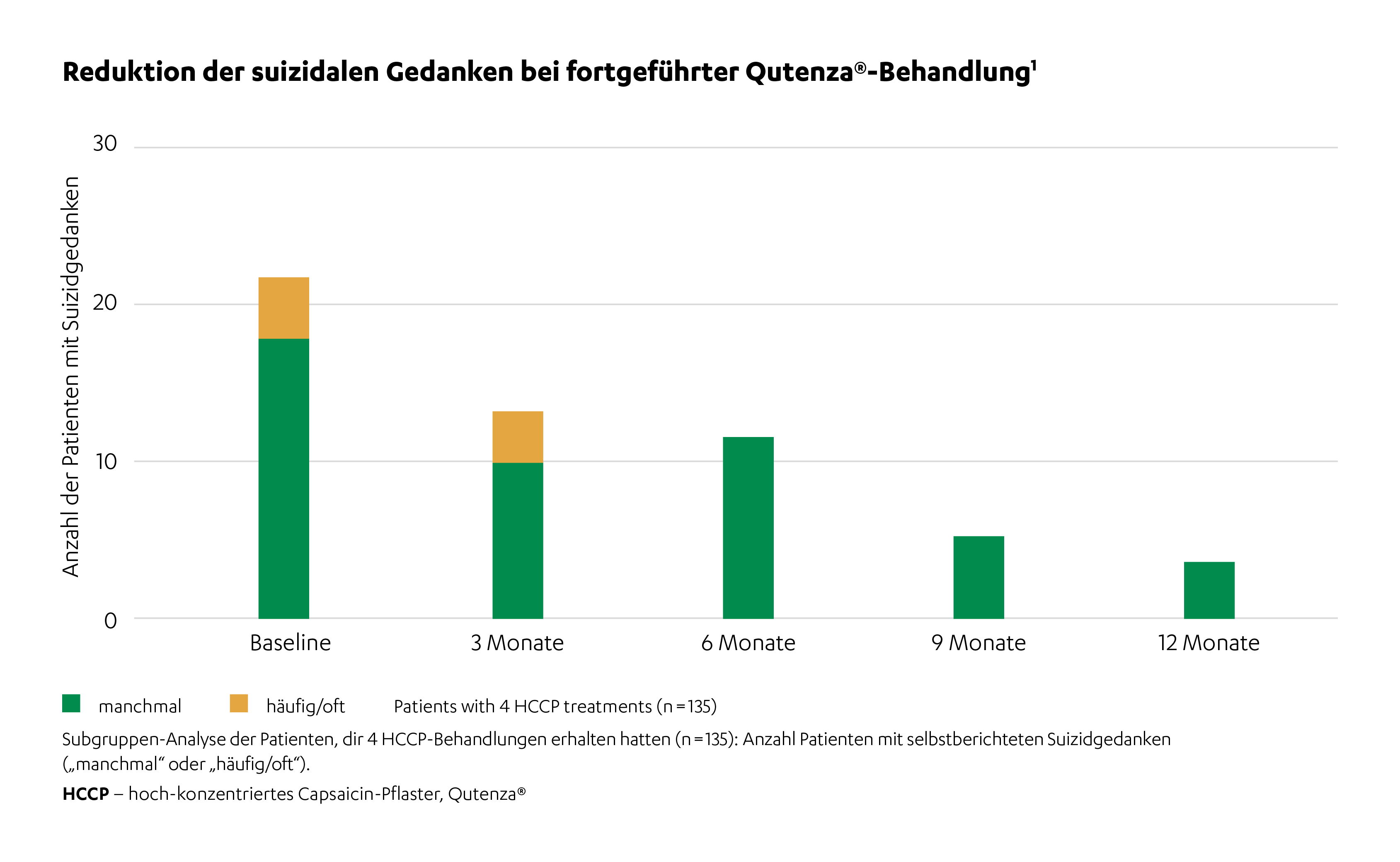
Im Verlauf der 12-monatigen Studie führte die QUTENZA®-Behandlung zu einer signifikanten und progressiven Reduktion von Depressions-, Angst- und Stresssymptomen (DASS-Score Fragebogen) bei vier Anwendungen. Bereits nach einer Behandlung zeigten sich Verbesserungen, die sich mit jeder weiteren Anwendung verstärkten. Patientinnen und Patienten, die alle vier HCCP-Behandlungen abschlossen, wiesen hochsignifikante Verbesserungen in allen DASS-21-Subskalen sowie eine deutliche Abnahme suizidaler Gedanken auf. Demgegenüber verschlechterten sich die Symptome bei Personen, die die Behandlung abbrachen, was die Bedeutung der kontinuierlichen Therapie für die emotionale Stabilisierung unterstreicht.1

Die schmerzhafte diabetische Polyneuropathie(pDPN) ist eine...

QUTENZA® wirkt selektiv an den überaktiven Schmerzfasern, indem…

QUTENZA® ist eine Pflaster Therapie
zur lokalen Anwendung bei periphere...
M-QZA-CH-12-25-0010
Fachpersonen können bei Grünenthal Pharma AG eine vollständige Kopie der zitierten Referenz anfordern.
Kurz-Fachinformation QUTENZA®: Z: Kutanes Pflaster (280 cm2) mit 179 mg Capsaicin (8 % w/w). I: Behandlung von peripheren neuropathischen Schmerzen bei Erwachsenen, als Monotherapie oder in Kombination mit anderen Arzneimitteln gegen Schmerzen. D/A: QUTENZA® muss von einem Arzt oder einer medizinischen Fachkraft unter der Aufsicht eines Arztes angewendet werden. QUTENZA® sollte auf die schmerzhaftesten Hautareale (max. 4 Pflaster) aufgebracht werden. Vor dem Aufkleben des Pflasters kann das Behandlungsareal mit einem topischen Anästhetikum behandelt oder dem Patienten kann ein orales Analgetikum verabreicht werden. QUTENZA® kann auf die Grösse und Form der zu behandelnden Stelle zugeschnitten werden und soll an den Füssen 30 Minuten und an anderen Stellen 60 Minuten aufgeklebt bleiben. Die Behandlung mit QUTENZA® kann alle 90 Tage wiederholt werden. Erneute Behandlung nach weniger als 90 Tagen nur nach sorgfältiger Beurteilung durch den Arzt. Zwischen den Behandlungen ist ein Mindestintervall von 60 Tagen einzuhalten. KI: Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile des Arzneimittels oder Bestandteile des Reinigungsgels. VM: Beim Umgang mit den Pflastern und der Reinigung der Behandlungsstellen müssen Nitrilhandschuhe getragen werden. Der Gebrauch von Schutzmasken und Schutzbrillen wird empfohlen. Es empfiehlt sich, die Behandlung mit QUTENZA® in einem gut belüfteten Raum durchzuführen. QUTENZA® darf nur auf trockener, unversehrter Haut und nicht im Gesicht, über dem Haaransatz der Kopfhaut und/oder in der Nähe von Schleimhäuten angewendet werden. Ein unbeabsichtigter Kontakt mit den Pflastern oder anderen Materialien, die mit den behandelten Hautarealen in Kontakt waren, muss vermieden werden. UW: Die Nebenwirkungen treten nur vorübergehend auf, klingen von selbst wieder ab und sind gewöhnlich von leichter bis mässiger Intensität. Am häufigsten traten vorübergehendes lokales Brennen, Schmerzen (39.2 %), Erythem (32.8 %) und Pruritus an der Anwendungsstelle auf. Weitere häufige Nebenwirkungen: Hypertonie, Husten, Übelkeit, Schmerzen in Extremität, Muskelkrämpfe, Papeln, Bläschen, Ödem, Schwellung, Trockenheit, peripheres Ödem. P: QUTENZA® ist in einer Packung mit 1 oder 2 Pflaster und einer Tube Reinigungsgel (50 g) erhältlich. Abgabekategorie A. Ausführliche Angaben siehe www.swissmedicinfo.ch. Grünenthal Pharma AG, 8756 Mitlödi, Tel. 055 647 31 31. M-QZA-CH-11-24-0015